Ein mit 750.000 ausgestattetes britisch-schweizerisches Konsortium will die Kosten von Zell- und Gentherapien drastisch senken.
ANZEIGE
Schlagwortarchiv für: Gentherapie
Die US-amerikanische Zulassungsbehörde FDA hat der Bayer AG eine Schnellzulassung für AskBios Herzmittel AB-1002 in Aussicht gestellt.
Die Martinsrieder ViGeneron GmbH hat in einer klinischen Phase Ib-Studie den ersten Patienten mit intravitrealer Injektion von VG901 gegen Retinitis pigmentosa (RP) behandelt. Diese wird durch Mutationen im CNGA1-Gen verursacht. VG901 bringt ein funktionelles CNGA1-Gen in die Zielzellen der retinalen Photorezeptoren ein.
Rund 90 Mio. Euro investierte Roche in ein neues Entwicklungszentrum für Gentherapien. Am Standort Penzberg entwickelt und produziert das Unternehmen künftig Genvektoren für klinische Studien. Heute wurde das Zentrum eröffnet.
Die EMA hat die erste Gentherapie für die Erbkrankheit Sichelzellanämie zugelassen. Die Herstellung der Komponenten der auf einer CRISPR/Cas-Editing-Therapie basierenden Methode ähnelt dem Prinzip des Lego-Bausteins. Während die Bausteine verteilt in Europa hergestellt werden, setzt man bei der Nuklease Cas9 auf die Expertise von Biomay aus Wien.
„In keinem der analysierten Technologiefelder erreicht Deutschland eine international führende Wettbewerbsposition. Die Positionierung ist überwiegend durchschnittlich“, konstatiert die detaillierte Analyse von Innovationskraft im Pharmasektor und koppelt diesen mit der Diskussion über Abhängigkeiten. Der vfa sendet damit ein Alarmzeichen, da in seinen Augen Nichtstun den Abstand nur noch vergrößern werde.
Das an der Nasdaq notierte Biotech-Unternehmen CRISPR Therapeutics (Zug, Schweiz) hat mit seinem Partner Vertex Pharmaceuticals nach der Zulassung im Vereinigten Königreich auch von der US-amerikanischen Gesundheitsbehörde FDA die Zulassung für die Gentherapie Casgevy erhalten.
Der Schweizer MetrioPharm wurde von der FDA die Rare Pediatric Disease Designation (RPDD) für Duchenne-Muskeldystrophie (DMD) erteilt. Damit hat MetrioPharm Aussicht auf eine schnellere Begutachtung des Antrages und einen "Gutschein", der branchenüblich mit einem Marktwert von mehr als 100 Mio. US-Dollar hochgerechnet wird. Erst kürzlich hatte das Unternehmen 18 Mio. Schweizer Franken in einer Serie D-Finanzierungsrunde für die Entwicklung des Wirkstoffes erhalten und strebt eine zweite Finanzierungsrunde an.
Positive Phase I-Daten der US-Tochter Bluerock Therapeutics LP bei Parkinson lassen die Leverkusener hoffen. Die Gentherapie wurde vor allem auf ihre Anwendungssicherheit getestet und zeigte keine unerwünschten Nebenwirkungen. Zudem deuten die Daten auf eine leichte Verbesserung der klinischen Symptome in der höchsten Dosierung hin. Die guten Nachrichten bei Bayer Pharma heizen die Gerüchte um eine Aufspaltung in ein Gesundheits- und ein Agrarunternehmen erneut an.
Die Heidelberger AaviGen GmbH erhält 17 Mio. Euro für die Erforschung der Präzisionsgentherapie bei Herzinsuffizienz in einer Serie B-Finanzierung. Dass diese von Dietmar Hopp getragen wird, lässt aufhorchen.


 Bayer
Bayer Roche
Roche Biomay AG
Biomay AG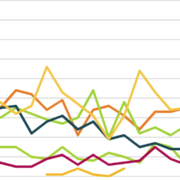 ©vfa
©vfa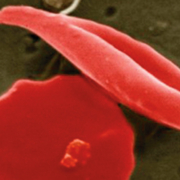 © wikipedia.org/EM Unit, UCL Medical School, Royal Free Campus, Wellcome Images, CC 2.0
© wikipedia.org/EM Unit, UCL Medical School, Royal Free Campus, Wellcome Images, CC 2.0

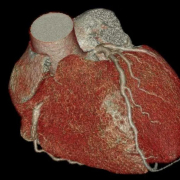 Universitätsklinikum Heidelberg
Universitätsklinikum Heidelberg